Вакцины – иммунобиологические препараты для иммунопрофилактики инфекционных заболеваний путем выработки активного иммунного ответа к конкретному возбудителю. Вакцинные средства помогают создать длительную устойчивость организма к определенной разновидности патогенных микробных тел. Вакцины помогают проводить плановую и экстренную профилактику инфекционных болезней, которая называется вакцинация. Эта эффективная и одновременно простая методика быстро завоевала уважение среди специалистов. Она служит для предупреждения эпидемий, угрожающих здоровью всего человечества.
Суть прививки
Вакцинация – план действий, направленных на обеспечение защиты организма взрослого или ребенка от вредоносных микроорганизмов. Метод основан на способности иммунобиологических растворов, тренировать иммунитет путем запоминания инфекционных агентов или анатоксинов и моментального их уничтожения при последующем инфицировании.
Прививка – многоуровневое действие, условно разделенное на несколько этапов:
- выявление лиц, которым рекомендована вакцинопрофилактика;
- выбор вакцинного препарата (живого, инактивированного, анатоксина);
- составление графика прививок;
- введение соответственно утвержденному плану вакцин;
- контроль результатов;
- предупреждение и лечение вероятных постпрививочных осложнений или побочных реакций (наиболее часто патологические реакции наблюдаются после введения анатоксинов столбняка, дифтерийной палочки в сочетании с коклюшным компонентом).
Современные вакцины – высокоэффективные и надежные препараты со специфическими антигенами (микроорганизмы, их фрагментарные части, анатоксины) для профилактики опасных инфекционных патологий и других заболеваний. Они создаются путем применения современных генно-инженерных разработок. Они способствуют быстрому формированию защитной устойчивости к разному роду болезненных состояний. Вакцины могут использоваться для вакцинотерапии заражения после контакта пациента с потенциальным возбудителем.
Основные способы иммунизации

Способы прививания зависят от метода введения профилактического раствора с антигенами человеку. В клинической практике применяют ряд этих методик. В зависимости от их особенностей определяют, каким способом будет происходить прививание иммунного ответа:
- внутримышечный метод предполагает необходимость произведения инъекции в мышцы бедра, дельты (яркий пример – прививка с анатоксинами АКДС);
- подкожные прививки ставят в подлопаточную или плечевую область (такой вариант прививки отличается повышенной результативностью, низкой аллергенностью, простотой использования);
- внутрикожные вакцинные инъекции проводятся живой вакциной (БЦЖ, чумы, туляремии, лихорадки Ку);
- ингаляционный метод используется при проведении экстренной помощи (таким путем вводятся вакцины против столбняка, гриппа, дифтерийной интоксикации, краснухи, туберкулеза);
- пероральный прием — один из самых удобных вариантов иммунизации, так как средства вводятся через рот в виде капель (прививка от бешенства, вакцина от полиомиелита).
Внутримышечные, подкожные, внутрикожные прививки являются самыми неприятными для пациентов, так как вводятся путем прокола кожных покровов, доставляя человеку боль. Для устранения неприятных ощущений сегодня рекомендуют вводить препараты в виде аэрозолей или через рот. Помимо безболезненности, данные способы профилактической иммунизации отличаются высокой стерильностью и небольшим количеством послепрививочных осложнений.
Классификация вакцин

В зависимости от происхождения существует четыре типа вакцин:
- живая вакцина, состоящая из ослабленных возбудителей;
- инактивированная суспензия, в состав которой входят убитые микроорганизмы или их фрагменты;
- химическая вакцина содержит высокоочищенные антигены;
- синтетическая вакцина, синтезированная с помощью передовых генно-инженерных технологий в сфере микробиологии.
Некоторые вакцины состоят из компонентов, способствующих выработке иммунитета против одного заболевания (монопрепараты). Другие включают действующие вещества, защищающие сразу от нескольких патологий, поэтому носят название комбинированные вакцины.
Если принять во внимание род антигенов, задействованных при создании вакцины, тогда несложно выделить типы растворов:
- содержащие целые микробные клеточные элементы (живая или инактивированная вакцина);
- включающие фрагменты микробных единиц;
- состоящие их токсинов микроорганизмов (анатоксины);
- созданные на основе синтетических антигенов;
- полученные путем синтеза антигенов с помощью достижений генной инженерии.
Что такое живая вакцина?

Классическая живая вакцина – средство иммунопрофилактики, в процессе изготовления которого использовались не полностью убитые, но ослабленные штаммы патогенных агентов. Эти препараты имеют выраженные иммуногенные свойства, но при этом не способны спровоцировать развитие болезни с присущей ему симптоматикой.
Введение такой разновидности вакцин провоцирует образование защитных комплексов, относящихся к стойкому клеточному, гуморальному или секреторному иммунитету. Эти суспензии нередко становятся причиной развития осложнений, в отличие от анатоксинов, гораздо лучше воспринимающихся иммунной сферой.
Преимущественные качества и недостатки
Среди плюсов вакцин, созданных с применением живых, то есть не убитых микробных агентов, выделяют:
- высокая эффективность;
- быстрое образование иммунных комплексов;
- отсутствие каких-либо консервантов в составе препарата;
- использование минимальных концентраций вакцин;
- возможность применения разных методик прививания;
- активация разных типов иммунитета;
- невысокая стоимость и доступность.
Живая вакцина, помимо преимуществ, имеет также свои недостатки. К основным минусам относят:
- способность провоцировать развитие патологии при вакцинации пациента с ослабленным иммунитетом;
- вакцины на основе живых возбудителей неустойчивы и быстро теряют свои положительные качества при температурных изменениях (люди сталкиваются с нежелательными эффектами иммунизации именно после введения некачественных вакцин);
- живую вакцину нельзя компоновать с другими средствами вакцинопрофилактики (подобные действия чреваты потерей эффекта от препаратов или появлением аллергии).
Разновидности вакцинных суспензий живого типа

Иммунологи учитывают свойства компонентов вакцин с живыми микробами, разделяя их на аттенуированные и дивергентные суспензии. Аттенуированные или ослабленные растворы создаются на основе болезнетворных штаммов с резко сниженной способностью вызывать болезнь, но не утративших своей иммуногенности. На введение данных вакцин иммунитет отвечает формированием антител к инфекции, не давая ей возможностей развиваться в будущем. Основная часть аттенуированных вакцин – препараты для профилактики бешенства, гриппа, Ку-лихорадки, паротита, кори, краснухи и разных штаммов аденовируса.
Вторая группа – вакцины из естественных (дивергентных) штаммов микроорганизмов, обладающих низкой вирулентностью по отношению к организму, но способные стимулировать синтез защитных антител. Примером таких растворов являются профилактические вакцины от натуральной оспы, изготовленные из вирусов коровьей оспы.
Особенности противогриппозной вакцины
Грипп является сложной вирусной болезнью, ежегодно поражающим сотни тысяч наших сограждан, вызывает огромное количество осложнений и даже может стать причиной летального исхода пациентов. Единственный путь предупреждения опасной инфекции – своевременное применение вакцины, помогающей создать кратковременный иммунитет, чего достаточно для предупреждения сезонной волны инфекции.
К главным показаниям к прививанию относятся:
- пожилой возраст (от 60 лет и старше);
- наличие у пациента хронических заболеваний органов бронхолегочной и сердечно-сосудистой системы;
- пациенты, страдающие тяжелыми патологиями печени и почек, люди с расстройствами метаболизма, иммуносупрессией;
- беременность после 12 недель.
Основные виды противогриппозных растворов

Вакцины, защищающие от гриппа, бывают живыми или инактивированными. Противогриппозных анатоксинов не существует. Инактивированные суспензии подразделяются:
- убитая вакцина, которая содержит неразрушенные, но высокоочищенные вирионы возбудителя;
- сплит-вакцина (расщепленная), состоящая из разрушенных вирусных агентов;
- субъединичная вакцина содержит фрагментарные белки оболочек вирусов, способных обеспечивать индукцию иммунных клеток.
В медицинской практике часто пользуются вакцинами из числа субъединичных растворов, так как они лишены куриного белка и являются адаптированными для человека. Самые известные представители этого ряда – популярные вакцины «Агриппал» и «Инфлювак».
1. По характеру антигена.
Бактериальные вакцины
Вирусные вакцины
2.По способам приготовления.
Живые вакцины
Инактивированные вакцины (убитые, неживые)
Молекулярные (анатоксины)
Генно-инженерные
Химические
3. По наличию полного или неполного набора антигенов.
Корпускулярные
Компонентные
4. По способности вырабатывать невосприимчивость к одному или нескольким возбудителям.
Моновакцины
Ассоциированные вакцины.
Живые вакцины – препараты в которых в качестве действующего начала используются:
Аттенуированные, т.е. ослабленные (потерявшие свою патогенность) штаммы микроорганизмов;
Так называемые дивергентные штаммы непатогенных микроорганизмов, имеющих родственные антигены с антигенами патогенных микроорганизмов;
Рекомбинантные штаммы микроорганизмов, полученные генно-инженерным способом (векторные вакцины).
Иммунизация живой вакциной приводит к развитию вакцинального процесса, протекающего у большинства привитых без видимых клинических проявлений. Основное достоинство этого типа вакцин – полностью сохраненный набор антигенов возбудителя, что обеспечивает развитие длительной невосприимчивости даже после однократной иммунизации. Однако есть и ряд недостатков. Главный – риск развития манифестной инфекции в результате снижения аттенуации вакцинного штамма (напр., живая полиомиелитная вакцина в редких случаях может вызвать полиомиелит вплоть до развития поражения спинного мозга и паралича).
Аттенуированные вакцины изготавливают из микроорганизмов с пониженной патогенностью, но выраженной иммуногенностью. Введение их в организм имитирует инфекционный процесс.
Дивергентные вакцины – в качестве вакцинных штаммов используются микроорганизмы, находящиеся в близком родстве с возбудителями инфекционных заболеваний. Антигены таких микроорганизмов индуцируют иммунный ответ, перекрестно направленный против антигенов возбудителя.
Рекомбинантные (векторные) вакцины – создаются на основе использования непатогенных микроорганизмов со встроенными в них генами специфических антигенов патогенных микроорганизмов. В результате этого введенный в организм живой непатогенный рекомбинантный штамм вырабатывает антиген патогенного микроорганизма, обеспечивающий формирование специфического иммунитета. Т.о. рекомбинантный штамм выполняет роль вектора (проводника) специфического антигена. В качестве векторов используют, например, ДНК-содержащий вирус осповакцины, непатогенные сальмонеллы, в геном которых введены гены HBs – антигена вируса гепатита В, антигены вируса клещевого энцефалита и др.
|
Бактериальные вакцины |
Наименование вакцины |
Штамм | |
|
Туберкулезная, БЦЖ (из микобактерий бычьего типа) |
Атт., Див. |
А.Кальмет, К.Герен |
|
|
Чумная, EV |
Г.Жирар, Ж.Робик |
||
|
Туляремийная |
Б.Я.Эльберт, Н.А.Гайский |
||
|
Сибиреязвенная, СТИ |
Л.А.Тамарин, Р.А.Салтыков |
||
|
Бруцеллезная |
П.А.Вершилова |
||
|
Ку-лихорадки, М-44 |
В.А.Гениг, П.Ф.Здродовский |
||
|
Вирусные вакцины |
Оспенная (вирус оспы коров) |
Э.Дженнер |
|
|
А.А.Смородинцев, М.П.Чумаков |
|||
|
Желтой лихорадки | |||
|
Гриппозная |
В.М.Жданов |
||
|
Паротитная |
А.А.Смородинцев, Н.С.Клячко |
||
|
Венесуэльского энцефаломиелита |
В.А.Андреев, А.А.Воробьев |
||
|
Полиомиелитная |
А.Сэбин, М.П.Чумаков, А.А.Смородинцев |
Примечание: Атт. – аттенуированная, Див. – дивергентная.
Инактивированные вакцины – приготовлены из убитых микробных тел либо метаболитов, а также отдельных антигенов, полученных биосинтетическим или химическим путем. Эти вакцины проявляют меньшую (по сравнению с живыми) иммуногенность, что ведет к необходимости многократной иммунизации, однако они лишены балластных веществ, что уменьшает частоту побочных эффектов.
Корпускулярные (цельноклеточные, цельновирионные) вакцины – содержат полный набор антигенов, приготовлены из убитых вирулентных микроорганизмов (бактерий или вирусов) путем термической обработки, либо воздействием химических агентов (формалин, ацетон). Напр., противочумная (бактериальная), антирабическая (вирусная).
Компонентные (субъединичные)вакцины – состоят из отдельных антигенных компонентов, способных обеспечить развитие иммунного ответа. Для выделения таких иммуногенных компонентов используют различные физико-химические методы, поэтому их ещё называют химические вакцины. Напр., субъединичные вакцины против пневмококков (на основе полисахаридов капсул), брюшного тифа (на основе О-, Н-, Vi - антигенов), сибирской язвы (полисахариды и полипептиды капсул), гриппа (вирусные нейраминидаза и гемагглютинин). Для придания этим вакцинам более высокой иммуногенности их сочетают с адъювантами (сорбируют на гидроксиде аллюминия).
Генно-инженерные вакцины содержат антигены возбудителей, полученные с использованием методов генной инженерии, и включают только высокоиммуногенные компоненты, способствующие формированию иммунного ответа.
Пути создания генно-инженерных вакцин:
1. Внесение генов вирулентности в авирулентные или слабовирулентные микроорганизмы (см. векторные вакцины).
2. Внесение генов вирулентности в неродственные микроорганизмы с последующим выделением антигенов и их использованием в качестве иммуногена. Напр., для иммунопрофилактики гепатита В предложена вакцина, представляющая собой HBsAg вируса. Его получают из дрожжевых клеток, в которые введен вирусный ген (в форме плазмиды), кодирующий синтез HBsAg. Препарат очищают от дрожжевых белков и используют для иммунизации.
3. Искусственное удаление генов вирулентности и использование модифицированных организмов в виде корпускулярных вакцин. Селективное удаление генов вирулентности открывает широкие перспективы для получения стойко аттенуированных штаммов шигелл, токсигенных кишечных палочек, возбудителей брюшного тифа, холеры и др. бактерий. Возникает возможность для создания поливалентных вакцин для профилактики кишечных инфекций.
Молекулярные вакцины – это препараты в которых антиген представлен метаболитами патогенных микроорганизмов, чаще всего молекулярных бактериальных экзотоксинов – анатоксинов.
Анатоксины – токсины обезвреженные формальдегидом (0,4%) при 37-40 ºС в течение 4 нед., полностью утратившие токсичность, но сохранившие антигенность и иммуногенность токсинов и используемые для профилактики токсинемических инфекций (дифтерии, столбняка, ботулизма, газовой гангрены, стафилококковых инфекций и др.). Обычный источник токсинов –промышленно култивируемые естественные штаммы-продуценты. Анатоксины выпускаю в форме моно- (дифтерийный, столбнячный, стафилококковый) и ассоциированных (дифтерийно-столбнячный, ботулинический трианатоксин) препаратов.
Конъюгированные вакцины – комплексы бактериальных полисахаридов и токсинов (напр., сочетание антигенов Haemophilus influenzae и дифтерийного анатоксина). Принимаются попытки создать смешанные бесклеточные вакцины, включающие анатоксины и некоторые другие факторы патогенности, напр., адгезины (напр., ацеллюлярная коклюшно-дифтерийно-столбнячная вакцина).
Моновакцины – вакцины применяемые для создания невосприимчивости к одному возбудителю (моновалентные препараты).
Ассоциированные препараты – для одномоментного создания множественной невосприимчивости, в этих препаратах совмещаются антигены нескольких микроорганизмов (как правило убитых). Наиболее часто применяются: адсорбированная коклюшно-дифтерийно-столбнячная вакцина (АКДС-вакцина), тетравакцина (вакцина против брюшного тифа, паратифов А и В, столбнячный анатоксин), АДС-вакцина (дифтерийно-столбнячный анатоксин).
Методы введения вакцин.
Вакцинные препараты вводят внутрь, подкожно, внутрикожно, парентерально, интраназально и ингаляционно. Способ введения определяют свойства препарата. Живые вакцины можно вводить накожно (скарификацией), интраназально или перорально; анатоксины вводят подкожно, а неживые корпускулярные вакцины – парентерально.
Внутримышечно вводят (после тщательного перемешивания) сорбированные вакцины (АКДС, АДС, АДС-М, ВГВ, ИПВ). Верхний наружный квадрант ягодичной мышцы использоваться не должен, так как у 5% детей там проходит нервный ствол, а ягодицы грудничка бедны мышцами, так что вакцина может попасть в жировую клетчатку (риск медленно рассасывающейся гранулемы). Место инъекции - передненаружная область бедра (латеральная часть четырехглавой мышцы) или, у детей старше 5-7 лет, дельтовидная мышца. Игла вводится отвесно (под углом 90°). После укола следует оттянуть поршень шприца и вводить вакцину только при отсутствии крови, в противном случае следует повторить укол. Перед инъекцией собирают мышцу двумя пальцами в складку, увеличив расстояние до надкостницы. На бедре толщина подкожного слоя у ребёнка до возраста 18 месяцев - 8 мм (макс. 12 мм), а толщина мышцы - 9 мм (макс. 12 мм), так что достаточно иглы длиной 22-25 мм. Другой метод - у детей с толстой жировой прослойкой - растянуть кожу над местом инъекции, сократив толщину подкожного слоя; при этом глубина введения иглы меньше (до 16 мм). На руке толщина жирового слоя всего 5-7 мм, а толщина мышцы - 6-7 мм. У больных гемофилией внутримышечное введение осуществляют в мышцы предплечья, подкожное - в тыл кисти или стопы, где легко прижать инъекционный канал. Подкожно вводят несорбированные - живые и полисахаридные - вакцины: в подлопаточную область, в наружную поверхность плеча (на границе верхней и средней трети) или в передненаружную область бедра. Внутрикожное введение (БЦЖ) проводят в наружную поверхность плеча, реакция Манту - в сгибательную поверхность предплечья. ОПВ вводят в рот, в случае срыгивания ребенком дозы вакцины ему дают повторную дозу, если он срыгнет и ее, - вакцинацию откладывают.
Наблюдение за привитыми длится 30 минут, когда теоретически возможна анафилактическая реакция. Следует информировать родителей о возможных реакциях, требующих обращения к врачу. Ребенок наблюдается патронажной сестрой первые 3 дня после введения инактивированной вакцины, на 5-6-й и 10-11-й день - после введения живых вакцин. Сведения о проведенной вакцинации заносят в учетные формы, прививочные журналы и в Сертификат профилактических прививок.
По степени необходимости выделяют: плановую (обязательную) вакцинацию, которая проводится в соответствии с календарем прививок и вакцинацию по эпидемиологическим показаниям, которая проводится для срочного создания иммунитета у лиц, подвергшихся риску развития инфекции.
КАЛЕНДАРЬ ПРОФИЛАКТИЧЕСКИХ ПРИВИВОК В УКРАИНЕ
(Приказ МЗ Украины №48 от 03.02.2006)
Прививки по возрасту
|
Возраст |
Вакцинация от: |
Примечания |
|
Гепатит В | ||
|
Туберкулеза | ||
|
Гепатит В | ||
|
Дифтерии, Коклюша, Столбняка Полиомиелита (ИПВ) Гемофильной инфекции |
Детям с высоким риском развития поствакцинальных осложнений вакциной АаКДС |
|
|
Дифтерии, Коклюша, Столбняка Полиомиелита (ОПВ) Гемофильной инфекции |
Детям с высоким риском развития поствакцинальных осложнений вакциной АаКДС |
|
|
Гепатит В | ||
|
Кори, Краснухи,Паротита | ||
|
Дифтерии, Коклюша, Столбняка вакциной АаКДС Полиомиелита (ОПВ) Гемофильной инфекции | ||
|
Дифтерии, Столбняка Полиомиелита (ОПВ) Кори, Краснухи, Паротита | ||
|
Туберкулеза | ||
|
Дифтерии, Столбняка Полиомиелита (ОПВ) Туберкулеза | ||
|
Краснухи (девочки), Паротита (мальчики) | ||
|
Дифтерии, Столбняка | ||
|
Взрослые |
Дифтерии, Столбняка |
Прививки для профилактики туберкулеза не проводят в один день с другими прививками. Недопустимо комбинировать в один день прививки для профилактики туберкулеза с другими парентеральными манипуляциями. Ревакцинации против туберкулеза подлежат дети в возрасте 7 и 14 лет с негативным результатом пробы Манту. Ревакцинация проводится вакциной БЦЖ.
Вакцинации для профилактики гепатита В подлежат все новорожденные, вакцинация проводится моновалентной вакциной (Энжерикс В). Если мать новорожденного HBsAg «–» (негативна), что документально подтверждено, можно начать вакцинацию ребенка в течение первых месяцев жизни или объединить с прививками против коклюша, дифтерии, столбняка, полиомиелита (Инфанрикс ИПВ, Инфанрикс пента). В случае комбинации иммунизации с прививками против коклюша, дифтерии, столбняка и полиомиелита, рекомендуются схемы: 3-4-5-18 мес жизни или 3-4-9 мес. жизни. Если мать новорожденного HBsAg «+» (позитивна), ребенка прививают по схеме (первые сутки жизни) - 1-6 мес. Первая доза вводится в первые 12 часов жизни ребенка независимо от массы тела. Вместе с вакцинацией, но не позже 1-ой недели жизни, в другую часть тела необходимо ввести специфичный иммуноглобулин против гепатита В из расчета 40 МЕ/кг массы тела, но не менее 100 МЕ. Если у матери новорожденного с HBsAg неопределен HBsAg статус, прививки ребенку проводят обязательно в первые 12 часов жизни с одновременным исследованием статуса матери по HBsAg. В случае получения позитивного результата у матери, профилактику гепатита В проводят также как в случае прививки новорожденного ребенка от HBsAg «+» матери.
Интервал между первой и второй, второй и третьей вакцинацией АКДС вакциной составляет 30 дней. Интервал между третьей и четвертой вакцинацией должен составлять не менее 12 мес. Первая ревакцинация в 18 месяцев проводится вакциной с ацеллюлярным коклюшным компонентом (далее - АаКДС) (Инфанрикс). АаКДС используется для дальнейшей вакцинации детей, которые имели поствакцинальные осложнения на предыдущие прививки АКДС, а также для проведения всех вакцинаций детям с высоким риском возникновения поствакцинальных осложнений по итогам вакцинальной комисии или детского иммунолога. Для профилактики дифтерии, столбняка, коклюша, полиомиелита, гепатита В и инфекций вызванных бактериями Haemophilus influenze типа b (далее - Hib) можно использовать комбинированные вакцины (с разными вариантами комбинаций антигенов), которые зарегистрированы в Украине (Инфанрикс гекса).
Инактивированная вакцина для профилактики полиомиелита (далее ИПВ) применяется для первых двух вакцинаций, а в случае противопоказаний к введению оральной полиомиелитной вакцины (далее - ОПВ) - для всех последующих вакцинаций согласно календаря вакцинаций (Полиорикс, Инфанрикс ИПВ, Инфанрикс пента, Инфанрикс гекса). После вакцинации ОПВ предлагается ограничить инъекции, парентеральные вмешательства, плановые операции в течение 40 дней, исключить контакт с больными и ВИЧ-инфицированными.
Вакцинация для профилактики Hib-инфекции, может проводиться моновакцинами и комбинированными вакцинами которые содержат Hib-компонент (Хиберикс). В случае использования Hib-вакцины и АКДС разных производителей, вакцины вводятся в различные части тела. Желательно использовать комбинированные вакцины с Hib-компонентом для первичной вакцинации (Инфанрикс гекса).
Вакцинация для профилактики кори, эпидемического паротита и краснухи проводится комбинированной вакциной (далее - КПК) в возрасте 12 мес (Приорикс). Повторную вакцинацию для профилактики кори, паротита и краснухи проводят детям в возрасте 6 лет. Детям, которые не были вакцинированы против кори, паротита и краснухи в возрасте 12 мес и в 6 лет, вакцинацию можно провести в любом возрасте до 18 лет. В таком случае ребенок должен получить 2 дозы с минимальным интервалом. Детям в возрасте 15 лет, которые получили 1 или 2 вакцинацию против кори, но не были вакцинированы против эпидемического паротита и краснухи и не болели этими инфекциями, проводится плановая вакцинация против эпидемического паротита (мальчики) или против краснухи (девочки). Лица старше 18 лет, которые не были ранее вакцинированы против этих инфекций, могут быть вакцинированы одной дозой согласно эпидемическим показаниям в любом возрасте до 30 лет. Перенесенные заболевания корью, эпидемическим паротитом или краснухой не является противопоказанием к вакцинации тривакциной.
Ребёнка рожала в России и в роддоме малышу сразу поставили БЦЖ ипрививкуот гепатита В. Первые два месяца вакцинацию не проводили, был мед.отвод из-за желтушки. В три месяца вернулись в Японию, где постоянно проживаем. Здесь в три и четыре месяца поставили по три прививки: АКДС, от пневмонии, от гриппа (инфлюэнция b). Здесь совершенно другой календарь прививок и в связи с этим два вопроса: когда нам делать вторую и третью прививки гепатита В? Можно ли ставить 4 прививки за раз (здесь делают именно так)?
Согласно рекомендациям ВОЗ, одновременно можно вводить несколько вакцин, только в разные участки тела. Против гепатита В вы можете сделать 2 вакцинацию в 5 месяцев, а третью в 6 месяцев, прививку можно сочетать с другими вакцинами. Согласно японскому календарю прививок вакцинация проводится трехкратно по схеме сходной с российской 0-1 (4 недели)- 6 месяцев(20, 24 недели). Уточните для себя, может быть вас уже прививали от вирусного гепатита В?
Дочке 3 года и 3 месяца, прививки не ставили. Сейчас идет в сад, где детям в группе капают ОПВ (полиомиелит). Решили тоже привить дочь. В поликлинике предложили сразу привить каплями живой вакцины, ссылаясь на возраст дочери. Насколько безопасно так прививать ребенка? И могу ли я требовать поставить дочери ИПВ (2 укола с перерывом 45 дней)?
Отвечает Харит Сусанна Михайловна
Согласно национальному календарю прививок первые две прививки против полиомиелита должны быть инактивированными независимо от возраста. Делайте первые 2 прививки ИПВ с интервалом 1,5 месяца, затем - ОПВ. Ребенок дошкольного возраста должен быть привит как минимум трижды для защиты от полиомиелита, а также иметь 2 ревакцинации через 1 год.
Ребенку 1 г 10 мес. В 6 мес. была сделана прививка Инфанрикс-Гекса, две недели назад прививка корь-краснуха-паротит. Ребенок начал ходить в детский сад, сейчас узнала, что в группе есть дети, которым некоторое время назад сделали живую вакцину от полиомиелита.
Представляет ли пребывание с такими детьми опасность для моего ребенка?
Когда и какую можно сделать прививку от полиомиелита нам сейчас? У меня выбор: поставить комплексную АКДС Инфанрикс или только полиомиелит, можно ли сделать прививку от полиомиелита через две недели после Приорикса?
Отвечает Харит Сусанна Михайловна
Для защиты от любых форм полиомиелита ребенок должен иметь как минимум 3 прививки. При вакцинации других детей живой оральной вакциной против полиомиелита непривитые или не полностью привитые дети высаживаются из детского сада на 60 дней для предупреждения развития вакциноассоциированного полиомиелита.
Нет, через 2 недели вы не можете начать прививки, интервал между прививками не меньше 1 месяца. Вам нужно сделать как минимум 2 прививки против полиомиелита прежде, чем ребенок будет защищен от этой инфекции. Т.е если ребенок привит дважды, то только через 1 месяц после последней прививки выработается достаточный иммунитет. Лучше привиться 2-х кратно с интервалом в 1,5 месяца АКДС+ ИПВ(Пентаксим, ИнфанриксГекса), через 6-9 месяцев делается ревакцинация. АКДС+ИПВ/ОПВ(Пентаксим). Прививка против гепатита В у вас пропала, но если вы будете прививаться ИнфанриксГекса дважды с интервалом в 1,5 месяца, 3ю прививку против гепатита В можно сделать через 6 месяцев от первой. Рекомендую сделать полный курс вакцинации, поскольку ребенок посещает детский сад (организованный коллектив) и практически не имеет никакой защиты от опасных и тяжелых инфекций.
Получилось так, что моей дочке сделали прививку в 1,7 АКДС и полиомиелит (ходил муж и должны были делать только АКДС), а ровно через месяц ей снова дали капли от полиомиелита. Т.е. между двумя прививками полиомиелита прошёл месяц, а не 2 - как положено! Ребёнок чувствует себя хорошо. Но я очень переживаю за здоровье дочки и за саму ситуацию. Чем это может грозить и как дальше прививать?
Отвечает Харит Сусанна Михайловна
Ничего страшного не произойдет. Прививайтесь дальше по календарю. Такая схема используется по эпидпоказаниям. Вакцина безопасна и переносится хорошо.
В 8мес. ребенку поставили прививку от пневмококка и менее чем через месяц она заболела пневмонией! Есть ли связь между прививкой и болезнью? Теперь боюсь ставить прививку от гемофильной инфекции, которую предложили нам только в 1г 10 месяцев.
Отвечает Харит Сусанна Михайловна
Для защиты от пневмококковой инфекции ребенок раннего возраста должен быть привит как минимум 2-х кратно на первом году жизни и ревакцинирован после года, вот тогда иммунитет способен справиться с пневмококковой инфекцией. Однократная вакцинация не защищает от инфицирования. Необходимо было начать прививаться согласно календарю прививок в 2 и 4,5 месяца и тогда к 9 месяцам ребенок был бы защищен. Также, не забывайте, что кроме пневмококка пневмонию вызывают другие бактериальные и вирусные инфекции. Связи между вакцинацией и пневмонией нет, прививка могла вызвать лихорадку или недомогание (беспокойство, вялость) в течение 3 дней, а никак ни ОРЗ или пневмонию через 1 месяц от вакцинации. Прививайтесь от гемофильной инфекции тип В в 1 г 10 мес., прививка проводится однократно, ребенок будет защищен уже через 1 месяц после вакцинации.
Ребенку 3г.11мес., из прививок только БЦЖ, которую делали в роддоме. Планируем прививку в ближайшие дни, что лучше сделать, по вашему мнению: АДС + отдельно полиомиелит, или первую вакцинацию Пентаксимом (знаю что он показан до 4 лет), а далее уже АДС. Или можно, не смотря на возраст, сделать все четыре вакцинации Пентаксимом?
Отвечает Харит Сусанна Михайловна
Перед прививками необходима реакция Манту(если не делали), в день проверки можно начать прививаться.
Можно сделать Пентаксим, чтобы привиться сразу в т.ч. против гемофильной инфекции тип В, а далее - АДС и против полиомиелита (ИПВ), 2 прививка против полиомиелита должна быть также инактивированной вакциной. Ожидается, что летом 2017 года появится вакцина Адацел, ею можно прививаться против коклюша детям после 4-х лет.
У дочери (1,5 года) был мед.отводот прививок, потом поранила пальчик и ей вводят ПСС (1 мл). Когда делать АКДС?
Отвечает Харит Сусанна Михайловна
Прививайтесь по календарю через 1 месяц.
Открытие метода вакцинации дало старт новой эре борьбы с болезнями.
В состав прививочного материала входят убитые или сильно ослабленные микроорганизмы либо их компоненты (части). Они служат своеобразным муляжом, обучающим иммунную систему давать правильный ответ инфекционным атакам. Вещества, входящие в состав вакцины (прививки), не способны вызвать полноценное заболевание, но могут дать возможность иммунитету запомнить характерные признаки микробов и при встрече с настоящим возбудителем быстро его определить и уничтожить.
Производство вакцин получило массовые масштабы в начале ХХ века, после того как фармацевты научились обезвреживать токсины бактерий. Процесс ослабления потенциальных возбудителей инфекций получил название аттенуации.
Сегодня медицина располагает более, чем 100 видами вакцин от десятков инфекций.
Препараты для иммунизации по основным характеристикам делятся на три основных класса.
- Живые вакцины. Защищают от полиомиелита, кори, краснухи, гриппа, эпидемического паротита, ветряной оспы, туберкулеза, ротавирусной инфекции. Основу препарата составляют ослабленные микроорганизмы - возбудители болезней. Их сил недостаточно для развития значительного недомогания у пациента, но хватает, чтобы выработать адекватный иммунный ответ.
- Инактивированные вакцины. Прививки против гриппа, брюшного тифа, клещевого энцефалита, бешенства, гепатита А, менингококковой инфекции и др. В составе мертвые (убитые) бактерии или их фрагменты.
- Анатоксины (токсоиды). Особым образом обработанные токсины бактерий. На их основе делают прививочный материал от коклюша, столбняка, дифтерии.
В последние годы появился еще один вид вакцин - молекулярные. Материалом для них становятся рекомбинантные белки или их фрагменты, синтезированные в лабораториях путем применения методов генной инженерии (рекомбининтная вакцина против вирусного гепатита В).
Схемы изготовления некоторых видов вакцин
Живые бактериальные
Схема подходит для вакцины БЦЖ, БЦЖ-М.
Живые противовирусные

Схема подходит для производства вакцин от гриппа, ротавируса, герпеса I и II степеней, краснухи, ветряной оспы.
Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться:
- куриные эмбрионы;
- перепелиные эмбриональные фибробласты;
- первичные клеточные культуры (куриные эмбриональные фибробласты, клетки почек сирийских хомячков);
- перевиваемые клеточные культуры (MDCK, Vero, MRC-5, BHK, 293).
Первичный сырьевой материал очищают от клеточного дебриса в центрифугах и с помощью сложных фильтров.
Инактивированные антибактериальные вакцины
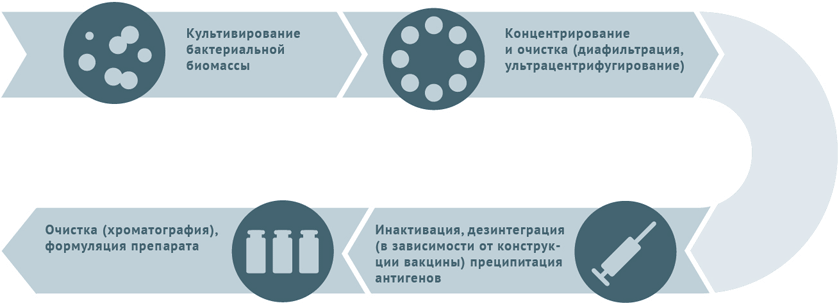
- Культивация и очистка штаммов бактерий.
- Инактивация биомассы.
- Для расщепленных вакцин клетки микробов дезинтегрируют и осаждают антигены с последующим их хроматографическим выделением.
- Для конъюгированных вакцин полученные при предыдущей обработке антигены (как правило, полисахаридные) сближают с белком-носителем (конъюгация).
Инактивированные противовирусные вакцины

- Субстратами для выращивания вирусных штаммов при производстве вакцин могут становиться куриные эмбрионы, перепелиные эмбриональные фибробласты, первичные клеточные культуры (куриные эмбриональные фибробласты, клетки почек сирийских хомячков), перевиваемые клеточные культуры (MDCK, Vero, MRC-5, BHK, 293). Первичная очистка для удаления клеточного дебриса проводится методами ультрацентрифугирования и диафильтрации.
- Для инактивации используются ультрафиолет, формалин, бета-пропиолактон.
- В случае приготовления расщепленных или субъединичных вакцин полупродукт подвергают действию детергента с целью разрушить вирусные частицы, а затем выделяют специфические антигены тонкой хроматографией.
- Человеческий сывороточный альбумин применяется для стабилизации полученного вещества.
- Криопротекторы (в лиофилизатах): сахароза, поливинилпирролидон, желатин.
Схема подходит для производства прививочного материала против гепатита А, желтой лихорадки, бешенства, гриппа, полиомиелита, клещевого и японского энцефалитов.
Анатоксины

Для дезактивации вредного воздействия токсинов используют методы:
- химический (обработка спиртом, ацетоном или формальдегидом);
- физический (подогрев).
Схема подходит для производства вакцин против столбняка и дифтерии.
По данным Всемирной Организации Здравоохранения (ВОЗ), на долю инфекционных заболеваний приходится 25 % от общего количества смертей на планете ежегодно. То есть инфекции до сих пор остаются в списке главных причин, обрывающих жизнь человека.
Одним из факторов, способствующих распространению инфекционных и вирусных заболеваний, являются миграция потоков населения и туризм. Перемещение человеческих масс по планете влияет на уровень здоровья нации даже в таких высокоразвитых странах, как США, ОАЭ и государства Евросоюза.
По материалам: «Наука и жизнь» № 3, 2006, «Вакцины: от Дженнера и Пастера до наших дней», академик РАМН В. В. Зверев, директор НИИ вакцин и сывороток им. И. И. Мечникова РАМН.
Задать вопрос специалисту
Вопрос экспертам вакцинопрофилактики
Вопросы и ответы
Вакцина "Менюгейт" зарегистрирована в России? С какого возраста разрешена к применению?
Да, зарегистрирована, вакцина – от менингококка С, сейчас также есть вакцина конъюгированная, но уже против 4 типов менингококков – А, С, Y, W135 – Менактра. Прививки проводят с 9 мес.жизни.
Муж транспортировал вакцину РотаТек в другой город.Покупая ее в аптеке мужу посоветовали купить охлаждающий контейнер,и перед поездкой его заморозить в морозильной камере,потом привязать вакцину и так ее транспортировать. Время в пути заняло 5 часов. Можно ли вводить такую вакцину ребенку? Мне кажется,что если привязать вакцину к замороженному контейнеру, то вакцина замерзнет!
Отвечает Харит Сусанна Михайловна
Вы абсолютно правы, если в контейнере был лед. Но если там была смесь воды и льда- вакцина не должна замерзать. Однако живые вакцины, к которым относится ротавирусная, не увеличивают реактогенность при температуре менее 0, в отличие от неживых, а, например, для живой полиомиелитной допускается замораживание до -20 град С.
Моему сыну сейчас 7 месяцев.
В 3 месяца у него случился отек Квинке на молочную смесь Малютка.
Прививку от гепатита сделали в роддоме, вторую в два месяца и третью вчера в семь месяцев. Реакция нормальная, даже без температуры.
Но вот на прививку АКДС нам устно дали медотвод.
Я за прививки!! И хочу сделать прививку АКДС. Но хочу сделать ИНФАНРИКС ГЕКСА. Живем в Крыму!!! В крыму ее нигде нет. Посоветуйте как поступить в такой ситуации. Может есть зарубежный аналог? Бесплатную делать категорически не хочу. Хочу качественную очищеную, что бы как монжно меньше риска!!!
В Инфанрикс Гекса содержится компонент против гепатита В. Ребенок полностью привит против гепатита. Поэтому в качестве зарубежного аналога АКДС можно сделать вакцину Пентаксим. Кроме того, следует сказать, что отек Квинке на молочную смесь не является противопоказанием к вакцине АКДС.
Подскажите, пожалуйста, на ком и как тестируют вакцины?
Отвечает Полибин Роман Владимирович
Как и все лекарственные препараты вакцины проходят доклинические исследования (в лаборатории, на животных), а затем клинические на добровольцах (на взрослых, а далее на подростках, детях с разрешения и согласия их родителей). Прежде чем разрешить применение в национальном календаре прививок исследования проводят на большом числе добровольцев, например вакцина против ротавирусной инфекции испытывалась почти на 70 000 в разных странах мира.
Почему на сайте не представлен состав вакцин? Почему до сих пор проводится ежегодная реакция Манту (зачастую не информативна), а не делается анализ по крови, например, квантифероновый тест? Как можно утверждать реакции иммунитета на введенную вакцину, если еще ни кому не известно в принципе, что такое иммунитет и как он работает, особенно если рассматривать каждого отдельно взятого человека?
Отвечает Полибин Роман Владимирович
Состав вакцин изложен в инструкциях к препаратам.
Реакция Манту. По Приказу № 109 «О совершенствовании противотуберкулезных мероприятий в Российской Федерациии» и Санитарным правилам СП 3.1.2.3114-13 "Профилактика туберкулеза", несмотря на наличие новых тестов, детям необходимо ежегодно делать реакцию Манту, но так как этот тест может давать ложноположительные результаты, то при подозрении на тубинфицирование и активную туберкулезную инфекцию проводят Диаскин-тест. Диаскин-тест является высоко чувствительным (эффективным) для выявления активной туберкулезной инфекции (когда идет размножение микобактерий). Однако полностью перейти на Диаскин-тест и не делать реакцию Манту фтизиатры не рекомендуют, так как, он не "улавливает" раннее инфицирование, а это важно, особенно для детей, поскольку профилактика развития локальных форм туберкулеза эффективна именно в раннем периоде инфицирования. Кроме того, инфицирование микобактерией туберкулеза необходимо определять для решения вопроса о ревакцинации БЦЖ. К сожалению, нет ни одного теста, который бы со 100% точностью ответил на вопрос, есть инфицирование микобактерией или заболевание. Квантифероновый тест также выявляет только активные формы туберкулеза. Поэтому при подозрении на инфицирование или заболевание (положительная реакция Манту, контакт с больным, наличие жалоб и пр.) используются комплексные методы (диаскин-тест, квантифероновый тест, рентгенография и др.).
Что касается «иммунитета и как он работает», в настоящее время иммунология - это высокоразвитая наука и многое, в частности, что касается процессов на фоне вакцинации – открыто и хорошо изучено.
Ребёнку 1 год и 8 месяцев, все прививки ставились в соответствии с календарем прививок. В том числе 3 пентаксима и ревакцинация в полтора года тоже пентаксим. В 20 месяцев надо ставить от полиомиелита. Очень всегда переживаю и отношусь тщательно к выбору нужных прививок, вот и сейчас перерыла весь интернет, но так и не могу решить. Мы ставили всегда инъекцию (в пентаксиме). А теперь говорят капли. Но капли-живая вакцина, я боюсь различных побочек и считаю, что лучше перестраховаться. Но вот читала, что капли от полиомиелита вырабатывают больше антител, в том числе и в желудке, то есть более эффективные, чем инъекция. Я запуталась. Поясните, инъекция менее эффективна (имовакс-полио, например)? Отчего ведутся такие разговоры? У каплей боюсь хоть и минимальный, но риск осложнения в виде болезни.
Отвечает Полибин Роман Владимирович
В настоящее время Национальный календарь прививок России предполагает комбинированную схему вакцинации против полиомиелита, т.е. только 2 первых введения инактивированной вакциной и остальные – оральной полиовакциной. Это связано с тем, чтобы полностью исключить риск развития вакциноассоциированного полиомиелита, который возможен только на первое и в минимальном проценте случаев на второе введение. Соответственно, при наличии 2-х и более прививок от полиомиелита инактивированной вакциной, осложнения на живую полиовакцину исключены. Действительно, считалось и признается некоторыми специалистами, что оральная вакцина имеет преимущества, так как формирует местный иммунитет на слизистых кишечника в отличие от ИПВ. Однако сейчас стало известно, что инактивированная вакцина в меньшей степени, но также формирует местный иммунитет. Кроме того, 5 введений вакцины против полиомиелита как оральной живой, так и инактивированной вне зависимости от уровня местного иммунитета на слизистых оболочках кишечника, полностью защищают ребенка от паралитических форм полиомиелита. В связи с вышесказанным вашему ребенку необходимо сделать пятую прививку ОПВ или ИПВ.
Следует также сказать, что на сегодняшний день идет реализация глобального плана Всемирной организации здравоохранения по ликвидации полиомиелита в мире, которая предполагает полный переход всех стран к 2019 году на инактивированную вакцину.
В нашей стране уже очень долгая история использования многих вакцин – ведутся ли долгосрочные исследования их безопасности и можно ли ознакомиться с результатами воздействия вакцин на поколения людей?
Отвечает Шамшева Ольга Васильевна
За прошлый век продолжительность жизни людей возросла на 30 лет, из них 25 дополнительных лет жизни люди получили за счет вакцинации. Больше людей выживают, они живут дольше и качественнее за счет того, что снизилось инвалидность из-за инфекционных заболеваний. Это общий ответ на то, как влияют вакцины на поколения людей.
На сайте Всемирной Организации Здравоохранения (ВОЗ) есть обширный фактический материал о благотворном влиянии вакцинации на здоровье отдельных людей и человечества в целом. Отмечу, что вакцинация –это не система верований, это - область деятельности, опирающаяся на систему научных фактов и данных.
На основании чего мы можем судить о безопасности вакцинации? Во-первых, ведется учет и регистрация побочных действий и нежелательных явлений и выяснение их причинно-следственной связи с применением вакцин (фармаконадзор). Во-вторых, важную роль в отслеживании нежелательных реакций играют постмаркетинговые исследования (возможного отсроченного неблагоприятного действия вакцин на организм), которые проводят компании - владельцы регистрационных свидетельств. И, наконец, проводится оценка эпидемиологической, клинической и социально-экономической эффективности вакцинации в ходе эпидемиологических исследований.
Что качается фармаконадзора, то у нас в России система фармаконадзора только формируется, но демонстрирует очень высокие темпы развития. Только за 5 лет число зарегистрированных сообщений о нежелательных реакциях на лекарственные средства в подсистему «Фармаконадзор» АИС Росздравнадзора выросло в 159 раз. 17 033 жалобы в 2013 году против 107 в 2008. Для сравнения – в США в год обрабатываются данные около 1 млн случаев. Система фармаконадзора позволяет отслеживать безопасность препаратов, накапливаются статистические данные, на основании которых может измениться инструкция по медицинскому применению препарата, препарат может быть отозван с рынка и т.п. Таким образом, обеспечивается безопасность пациентов.
И по закону «Об обращении лекарственных средств» от 2010 года врачи обязаны сообщать федеральным органам контроля обо всех случаях побочного действия лекарственных средств.
Вакцина- медицинский препарат, предназначенный для создания иммунитета к инфекционным болезням.
Классификации вакцин:
1. Живые вакцины - препараты, действующим началом в которых являются ослабленные тем или иным способом, потерявшие свою вирулентность, но сохранившие специфическую антигенность штаммы патогенных бактерий. Примером таких вакцин являются БЦЖ и вакцина против натуральной оспы человека, в качестве которой используется непатогенный для человека вирус оспы коров.
2. Инактивированные (убитые) вакцины – препараты, в качестве действующего начала включающие убитые химическим или физическим способом культуры патогенных вирусов или бактерий, (клеточные, вирионные) или же извлечённые из патогенных микробов комплексы антигенов, содержащие в своём составе проективные антигены (субклеточные, субвирионные вакцины). В препараты иногда добавляют консерванты и адъюванты.
Инактивированные вакцины получают путем воздействия на микроорганизмы химическим путем или нагреванием. Такие вакцины являются достаточно стабильными и безопасными, так как не могут вызвать реверсию вирулентности. Они часто не требуют хранения на холоде, что удобно в практическом использовании. Однако у этих вакцин имеется и ряд недостатков, в частности, они стимулируют более слабый иммунный ответ и требуют применения нескольких доз (бустерные иммунизации).
Они содержат либо убитый целый микроорганизм (например цельноклеточная вакцина против коклюша, инактивированная вакцина против бешенства, вакцина против вирусного гепатита А), либо компоненты клеточной стенки или других частей возбудителя, как например в ацеллюлярной вакцине против коклюша, коньюгированной вакцине против гемофилусной инфекции или в вакцине против менингококковой инфекции. Их убивают физическими (температура, радиация, ультрафиолетовый свет) или химическими (спирт, формальдегид) методами. Такие вакцины реактогенны, применяются мало (коклюшная, против гепатита А).
Инактивированные вакцины также являются корпускулярными. Анализируя свойства корпускулярных вакцин также следует выделить, как положительные так и их отрицательные качества. Положительные стороны: Корпускулярные убитые вакцины легче дозировать, лучше очищать, они длительно хранятся и менее чувствительны к температурным колебаниям. Отрицательные стороны: вакцина корпускулярная - содержит 99 % балласта и поэтому реактогенная, кроме того, содержит агент, используемый для умерщвления микробных клеток (фенол). Еще одним недостатком инактивированной вакцины является то, что микробный штамм не приживляется, поэтому вакцина слабая и вакцинация проводится в 2 или 3 приема, требует частых ревакцинаций (АКДС), что труднее в плане организации по сравнению с живыми вакцинами. Инактивированные вакцины выпускают как в сухом (лиофилизированном), так и в жидком виде.
3. Молекулярные вакцины – в них антиген находится в молекулярной форме или даже в виде фрагментов его молекул, определяющих специфичность т. е. в виде эпитопов, детерминант.
Корпускулярные вакцины – содержащие в своем составе протективный антиген
3. Анатоксины относятся к числу наиболее эффективных препаратов. Принцип получения – токсин соответствующей бактерии в молекулярном виде превращают в нетоксичную, но сохранившую свою антигенную специфичность форму путем воздействия 0.4% формальдегида при 37t в течение 3-4 недель, далее анатоксин концентрируют, очищают, добавляют адъюванты.
4. Синтетические вакцины. Молекулы эпитопов сами по себе не обладают высокой иммуногенностью для повышения их антигенных свойств эти молекулы сшиваются с полимерным крупномолекулярным безвредным веществом, иногда добавляют адъюванты.
5. Ассоциированные вакцины – препараты, включающие несколько разнородных антигенов.
Требования, предъявляемые к современным вакцинам:
Иммуногенность;
Низкая реактогенность (аллергенность);
Не должны обладать тератогенностью, онкогенностью;
Штаммы, из которых приготовлена вакцина, должны быть генетически стабильны;
Длительный срок хранения;
Технологичность производства;
Простота и доступность в применении.
Комбинированные вакцины
К комбинированным вакцинам относят искусственные вакцины. Они представляют собой препараты, состоящие из микробного антигенного компонента (обычно выделенного и очищенного или искусственно синтезированного антигена возбудителя) и синтетических полиионов (полиакриловая кислота и другие) - мощных стимуляторов иммунного ответа. Содержанием этих веществ они и отличаются от химических убитых вакцин.
Первая такая отечественная вакцина - гриппозная полимер-субъединичная ("Гриппол"), разработанная в Институте иммунологии МЗ РФ, уже внедрена в практику российского здравоохранения.
Для специфической профилактики инфекционных заболеваний, возбудители которых продуцируют экзотоксин, применяют анатоксины. Анатоксин - это экзотоксин, лишенный токсических свойств, но сохранивший антигенные свойства. В отличии от вакцин, при использовании которых у человека формируется антимикробный иммунитет, при введении анатоксинов формируется антитоксический иммунитет, так как они индуцируют синтез антитоксических антител - антитоксинов. В настоящее время применяются:
●
дифтерийный,
●
столбнячный,
●
ботулинический,
●
стафилококковый анатоксины,
●
холероген-анатоксин.
Вакцина АКДС (адсорбированная коклюшно-дифтерийно-столбнячная вакцина), в которой коклюшный компонент представлен убитой коклюшной вакциной, а дифтерийный и столбнячный - соответствующими анатоксинами,
Вакцина ТАВТе, содержащая О-антигены брюшнотифозных, паратифозных А и В бактерий, и столбнячный анатоксин,
Брюшнотифозная химическая вакцина с секстаанатоксином (смесь анатоксинов клостридий ботулизма типов А, В, Е, клостридий столбняка, клостридий перфрингенс типа А и эдематиенс - два последних микроорганизма - наиболее частые возбудители газовой гангрены), и другие.
В то же время АДС (дифтерийно-столбнячный анатоксин), часто используемый вместо АКДС при вакцинации детей, является просто комбинированным препаратом, а не ассоциированной вакциной, так как содержит только анатоксины.